Molaridad
La molaridad (M) es el número de moles de soluto por litro de solucion . Por ejemplo, si se disuelven 0,5 moles de soluto en 100 mL de disolución, se tiene una concentración de ese soluto de 0,5 M (0,5 molar). Para preparar una disolución de esta concentración normalmente se disuelve primero el soluto en un volumen menor, por ejemplo 30 mL, y se traslada esa disolución a un matraz aforado, para después rellenarlo con más disolvente hasta los 100 mL.

Es el método más común de expresar la concentración en química sobre todo cuando se trabaja con reacciones químicas y relaciones estequiométricas. Sin embargo, tiene el inconveniente de que el volumen cambia con la temperatura.
Molalidad
La molalidad (m) es el número de moles de soluto por kilogramo de solvente. Para preparar soluciones de una determinada molalidad en un disolvente, no se emplea un matraz aforado como en el caso de la molaridad, sino que se puede hacer en un vaso de precipitados y pesando con una balanza analítica, previo peso del vaso vacío para poderle restar el correspondiente valor.

La principal ventaja de este método de medida respecto a la molaridad es que como el volumen de una disolución depende de la temperatura y de la presión, cuando éstas cambian, el volumen cambia con ellas. Gracias a que la molalidad no está en función del volumen, es independiente de la temperatura y la presión, y puede medirse con mayor precisión.
Es menos empleada que la molaridad.
Normalidad
La normalidad (N) es el número de equivalentes (n) de soluto (st) por litro de disolución (sc).
Normalidad ácido-base
Es la normalidad de una solución cuando se la utiliza para una reacción como ácido o base. Por esto suelen titularse utilizando indicadores de pH.
En este caso, los equivalentes pueden expresarse de la siguiente forma:
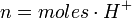 para un ácido, o
para un ácido, o  para una base.
para una base.
Donde:
- n: es la cantidad de equivalentes.
- moles: es la cantidad de moles.
- H+: Es la cantidad de protones cedidos por un mol del ácido.
- HO–: Es la cantidad de hidroxilos cedidos por un mol de la base.
Por esto, podemos decir lo siguiente:
 para un ácido, o
para un ácido, o  para una base.
para una base.
Donde:
- N: es la normalidad de la solución.
- M: es la molaridad de la solución.
- H+: Es la cantidad de protones cedidos por un mol del ácido.
- HO–: Es la cantidad de hidroxilos cedidos por un mol de la base.
Ejemplos:
- Una solución 1 M de HCl cede 1 M de H+, por lo tanto, es igual a 1 N.
- Una solución 1 M de Ca(OH)2 cede 2 M de HO–, por lo tanto, es igual a 2 N.
En este caso, los equivalentes pueden expresarse de la siguiente forma:
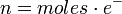 .
.
Donde:
- n: es la cantidad de equivalentes.
- moles: es la cantidad de moles.
- e–: Es la cantidad de electrones intercambiados en la hemireacción de oxidación o reducción.
Por esto, podemos decir lo siguiente:
 .
.
Donde:
- N: es la normalidad de la solución.
- M: es la molaridad de la solución.
- e–: Es la cantidad de electrones intercambiados en la hemireacción de oxidación o reducción.
Ejemplos:
- En el siguiente caso vemos que el anión nitrato en medio ácido (por ejemplo el ácido nítrico, puede actuar como oxidante, donde una solución 1 M, es 3 Nox.
- 4 H+ + NO3–1 + 3 e– ↔ NO + 2 H2O
- En el siguiente caso vemos que el anión ioduro, puede actuar como reductor, donde una solución 1 M, es 1 Nrd.
- 2 I– - 2 e– ↔ I2
- En el siguiente caso vemos que el catión argéntico, puede actuar como oxidante, donde una solución 1 M, es 1 Nox.
- 1 Ag+ + 1 e– ↔ Ag0


1 comentario:
omar ni siquiere te tomastela molestia de cambiar la letra que mal ehhh para eso me meto a wikipedia y lo copio de ahi eh????
como tu lo hiciste que feo....
Publicar un comentario